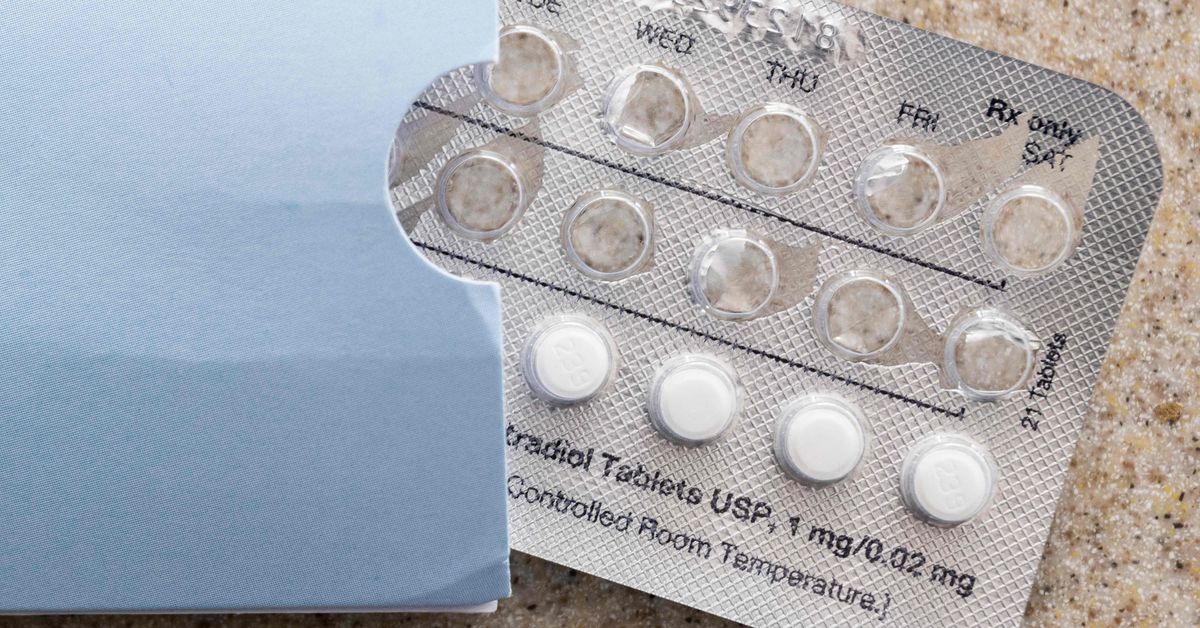
食品医薬品局は、最初の市販の経口避妊薬の申請を評価するように設定されています。 フランスの製薬会社HRAPharma 月曜日に言った FDAに避妊薬の認可を正式に要請したこと。
最高裁判所が中絶に対する連邦の保護を終了した後、米国が急速に変化するリプロダクティブヘルスケアの状況に取り組んでいるときに提出されます。 クラレンス・トーマス判事は最高裁判所の意見で、裁判所は避妊の権利に関する意見を再考すべきであると述べました。 タイミングは偶然です、HRAPharmaの最高戦略的オペレーションおよびイノベーションオフィサーであるFrédériqueWelgrynは 言った ニューヨークタイムズ。 「避妊は中絶へのアクセスの解決策ではありません」と彼女は言いました。 しかし、市販の避妊薬は避妊の障壁を取り除くのに役立つだろうと彼女は言った ステートメントで。
経口避妊薬のまれな副作用には血栓が含まれる可能性があり、血栓のリスクを高める病状(脳卒中の病歴など)のある人は、血栓を服用することをお勧めしません。 それが彼らが処方箋を必要とした理由の1つです。
HRA Pharmaの避妊薬は「ミニピル」であり、プロゲスチンとエストロゲンの組み合わせではなく、ホルモンのプロゲスチンのみが含まれています。 ミニピルは米国ではあまり使用されておらず、人々は毎日同じ時間に服用するように注意する必要があります。 しかし、エストロゲンが含まれていないため、血栓や脳卒中のリスクを高めることはありません。
米国医師会(AMA)のような組織は、市販の避妊薬をサポートしています。 「OTCに避妊薬へのアクセスを患者に提供することは、妊娠の健康リスクが経口避妊薬の使用のリスクをはるかに上回るため、公衆衛生の観点から簡単に呼び出すことができます」とAMA理事会メンバーのDavidAizussは声明で述べています。
別の製薬会社であるケイデンスヘルスも、市販の避妊薬に取り組んでいます。 その錠剤は、プロゲスチンとエストロゲンの組み合わせです。 両社はFDAと話し合っています 年。
FDAは 期待される HRAPharmaの申請を決定するのに約10か月かかります。